Đề thi thử THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Nguyễn Văn Linh (Có đáp án)
Bạn đang xem tài liệu "Đề thi thử THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Nguyễn Văn Linh (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề thi thử THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Nguyễn Văn Linh (Có đáp án)
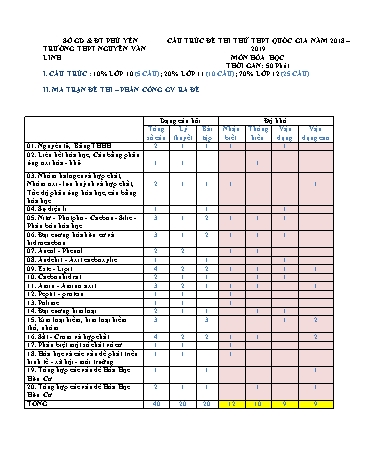
SỞ GD & ĐT PHÚ YÊN CẤU TRÚC ĐỀ THI THỬ THPT QUỐC GIA NĂM 2018 – TRƯỜNG THPT NGUYỄN VĂN 2019 LINH MÔN HÓA HỌC THỜI GAN: 50 Phút I. CẤU TRÚC : 10% LỚP 10 (5 CÂU); 20% LỚP 11 (10 CÂU); 70% LỚP 12 (25 CÂU) II. MA TRẬN ĐỀ THI – PHÂN CÔNG GV RA ĐỀ Dạng câu hỏi Độ khó Tổng Lý Bài Nhận Thông Vận Vận số câu thuyết tập biết hiểu dụng dụng cao 01. Nguyên tử, Bảng THHH 2 1 1 1 1 02. Liên kết hóa học, Cân bằng phản ứng oxi hóa - khử 1 1 1 03. Nhóm halogen và hợp chất, Nhóm oxi - lưu huỳnh và hợp chất, 2 1 1 1 1 Tốc độ phản ứng hóa học, cân bằng hóa học 04. Sự điện li 1 1 1 05. Nitơ - Photpho - Cacbon - Silic - 3 1 2 1 1 1 Phân bón hóa học 06. Đại cương hóa hữu cơ và 3 1 2 1 1 1 hiđrocacbon 07. Ancol - Phenol 2 2 1 1 08. Anđehit - Axit cacboxylic 1 1 1 09. Este - Lipit 4 2 2 1 1 1 1 10. Cacbonhiđrat 2 1 1 1 1 11. Amin - Amino axit 3 2 1 1 1 1 12. Peptit - protein 1 1 1 13. Polime 1 1 1 14. Đại cương kim loại 2 1 1 1 1 15. Kim loại kiềm, kim loại kiềm 3 3 1 2 thổ, nhôm 16. Sắt - Crom và hợp chất 4 2 2 1 1 2 17. Phân biệt một số chất vô cơ 1 1 1 18. Hóa học và các vấn đề phát triển 1 1 1 kinh tế - xã hội - môi trường 19. Tổng hợp các vấn đề Hóa Học 1 1 1 Hữu Cơ 20. Tổng hợp các vấn đề Hóa Học 2 1 1 1 1 Hữu Cơ TỔNG 40 20 20 12 10 9 9 21 Trường THPT Tôn Đức Thắng [email protected] DEON21 22 Trường THCS và THPT Nguyễn Bá Ngọc [email protected] DEON22 23 Trường THCS và THPT Chu Văn An [email protected] DEON23 24 Trường THCS&THPT Nguyễn Viết Xuân [email protected] DEON24 25 Trường THPT Nguyễn Thị Minh Khai [email protected] DEON25 26 Trường THPT Trần Bình Trọng [email protected] DEON26 27 Trường THPT Nguyễn Công Trứ [email protected] DEON27 28 Trường Phổ thông Duy Tân [email protected] DEON28 29 Trường THPT Nguyễn Bỉnh Khiêm [email protected] DEON29 30 Trường THPT Lê Thánh Tôn [email protected] DEON30 31 Trường THCS&THPT Võ Văn Kiệt [email protected] DEON31 32 Trường THCS và THPT Nguyễn Khuyến [email protected] DEON32 33 Trường THCS và THPT Võ Nguyên Giáp [email protected] DEON33 Hòa Hiệp trung ngày 06/ 09/ 2018 Trần Văn Mạnh A. Na3PO4: 50 g B. Na2HPO4: 15 g C. NaH2PO4: 49,2 g và Na2HPO4: 14,2 g D. Na2HPO4: 14,2 g và Na3PO4: 49,2 g Câu 9: Liên kết hoá học trong phân tử HCl là : A. liên kết ion. B. liên kết cộng hoá trị phân cực C. liên kết cho nhận. D. liên kết cộng hoá trị không phân cực. Câu 10: Công thức nào sau đây là công thức tổng quát của ankan? A. CnH2n-2 B. CnH2n-6 C. CnH2n+2 D. CnH2n Câu 11: 2,8 gam anken A làm mất màu vừa đủ dung dịch chứa 8 gam Br 2. Hiđrat hóa A chỉ thu được một ancol duy nhất. A có tên là: A. etilen. B. but - 2-en. C. hex- 2-en. D. 2,3-đimetylbut-2-en. Câu 12: Cho 3,36 lít khí hiđrocacbon X (đktc) phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Công thức phân tử của X là A. C4H6. B. C4H4. C. C2H2. D. C3H4. Giải: nX= 0,15 mol , nkết tủa= 36/0,15= 240 vậy C2H2. Câu 13: Cho biết sản phẩm chính của phản ứng khử nước của (CH3)2CHCH(OH) CH2 CH3 ? A. 2 - metylpent-1-en B. 3 - metylpent-1-en C. 2 - metylpent-2-en D. 4 - metylpent-2-en Câu 14: Ứng với công thức phân tử C7H18O có bao nhiêu đồng phân phenol ? A. 2B. 3 C. 4 D. 5 Câu 15: Este vinyl axetat có công thức là A. CH3COOCH=CH2. B. CH3COOCH3. C. CH2=CHCOOCH3. D. HCOOCH3. Câu 16: Hợp chất hữu cơ mạch hở X có công thức phân tử C6H10O4. Thủy phân X tạo ra hai ancol đơn chức có số nguyên tử cacbon trong phân tử gấp đôi nhau. Công thức của X là: A. CH3OCO–CH2–COOC2H5. B. C2H5OCO–COOCH3. C. CH3OCO–COOC3H7. D. CH3OCO–CH2–CH2–COOC2H5. Câu 17: Cho ancol X tác dụng với axit Y thu được este Z. Làm bay hơi 4,3 gam Z thu được thể tích hơi bằng thể tích của 1,6 gam oxi ở cùng điều kiện nhiệt độ, áp suất. Biết MX>My. Công thức của Z là: A. CH3COOCH=CH2 B. CH2=CH-COOCH3 C. HCOOCH=CH-CH3 D. HCOOCH2CH=CH2. Câu 25: Chất X có CT là C3H7O2N . X có thể tác dụng với NaOH , HCl và làm mất màu dd Br2. CT của X là: A. CH2 = CH COONH4 B. CH3CH(NH2)COOH C. H2NCH2CH2COOHD. CH 3CH2CH2NO2 Câu 26: Đốt cháy hoàn toàn 12,36 gam amino axit X có công thức dạng H 2NCxHy(COOH)t, thu được a mol CO2 và b mol H2O (b > a). Mặt khác, cho 0,2 mol X vào 1 lít dung dịch hỗn hợp KOH 0,4M và NaOH 0,3M, thu được dung dịch Y. Thêm HCl dư vào Y, thu được dung dịch 75,25 gam muối. Giá trị của b là A. 0,30.B. 0,42. C. 0,48.D. 0,54. Câu 27: Poli (metyl metacrylat) hay còn gọi là thủy tinh hữu cơ là một nhựa nhiệt déo trong suốt thường được sử dụng ở dạng tấm, miếng như một vật liệu nhẹ hoặc khó bể, vỡ để thay thế kính và thủy tinh silica. Thủy tinh hữu cơ được điều chế bằng cách: A. Cho metyl metacrylat phản ứng cộng với hidro B. Trùng hợp stiren C. Trùng hợp metyl metacrylat D. Trùng ngưng metyl metacrylat Câu 28: Cho CO dư qua ống sứ chứa hỗn hợp gồm MgO, Fe2O3, CuO, Al2O3 đun nóng. Phản ứng xong chất rắn thu được trong ống sứ là: A. MgO, Fe, Cu, Al B. MgO, Fe, Cu, Al2O3 C. Mg, Fe, Cu, Al2O3 D. Mg, Fe, Cu, Al Câu 29: Tiến hành điện phân dung dịch chứa m gam hỗn hợp CuSO4 và NaCl(H%= 100%, điện cực trơ, màng ngăn xốp)đến khi nước bắt đầu điện phân ở cả hai điện cực thì ngừng, thu được dung dịch X (Biết X làm phenolphtalein hóa hồng) và 8,96 lit khí (đktc) ở anot. Dung dịch X hòa tan tối đa 20,4 gam Al2O3. Giá trị m là: A. 123,7 B. 51,1 C. 78,8D. 67,1 Câu 30: Hòa tan hoàn toàn hỗn hợp K và Ca vào nước dư thu được dung dịch X và 3,36 lit khí ở đktc. Để trung hòa X cần V ml dung dịch (H2SO4 0,5M và HCl1M). Giá trị V là: A. 150B. 100 C. 75D. 300 Câu 31: Hòa tan hoàn toàn 3,79 gam hỗn hợp X gồm Al và Zn ( có tỉ lệ mol tương ứng 2:5) vào dung dịch chứa 0,394 mol HNO3 thu được dung dịch Y và V ml khí N2 duy nhất. Để phản ứng hết với các chất trong Y thu được dung dịch trong suốt cần 3,88 lit dung dịch NaOH 0,125M. Giá trị của V là: A. 352,8 B. 268,8 C. 358,4D. 112,0 Câu 32: X là dung dịch chứa a mol HCl. Y là dung dịch chứa b mol Na2CO3. Nhỏ từ từ hết X vàoY thu được V1 lit CO2 ở đktc. Nhỏ từ từ hết Y vào X thu được V2 lit CO2 ở đktc. Biết V1: V2 = 3:4. Tỉ lệ a:b là: A. 5:6B. 9:7C. 8:5D. 7:5 Câu 33: Chất nào có tính lưỡng tính: A. CrOB. Cr(OH) 2 C. Cr2O3 D. CrO3 Câu 34: Cho các chất FeO, Fe(NO3)2 , Fe2O3 , Fe3O4 , Fe(OH)3, FeSO4 , Fe2(SO4)3 lần lượt vào dung dịch HNO3. Số phản ứng oxihoa khử xảy ra là: A. 3B. 4C. 5D. 6 Câu 35: Cho m gam hỗn hợp Fe và Cu (Fe chiếm 80% về khối lượng) tác dụng với HNO3, kết thúc phản ứng thu được 0,1 gam chất rắn và 0,15 mol NO là sản phẩm khử duy nhất. Giá trị m gần nhất : A. 20,4B. 32,6C. 24,8D. 14,2 SỞ GD & ĐT PHÚ YÊN ĐỀ THI THỬ THPT QUỐC GIA NĂM 2018 – 2019 TRƯỜNG THPT NGUYỄN VĂN LINH MÔN HÓA HỌC THỜI GAN: 50 Phút Câu 1 : Nguyên tố Si có Z = 14. Cấu hình electron nguyên tử của silic là : A. 1s22s22p53s33p2 ;B. 1s 22s22p73s23p2 C. 1s22s32p63s23p2 D. 1s22s22p63s23p2. Câu 2 : Nguyên tố X có 3 đồng vị A 1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là: A. 27,28,32 B. 26,27, 34C. 28,29,30 D. 29,30,28 Câu 3: Tốc độ phản ứng là : A. Độ biến thiên nồng độ của một chất phản ứng trong một đơn vị thời gian. B. Độ biến thiên nồng độ của một sản phẩm phản ứng trong một đơn vị thời gian. C. Độ biến thiên nồng độ của một chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian. D. Độ biến thiên nồng độ của các chất phản ứng trong một đơn vị thời gian. Câu 4: Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na 2CO3 0,2M và NaHCO3 0,2M, sau phản ứng thu được số mol CO2 là A. 0,015 B. 0,020 C. 0,010 D. 0,030 Giải: 2 Khi cho H vào dung dịch hỗn hợp chứa CO3 và HCO3 thì: 2 Ban đầu: H CO3 HCO3 Nếu H dư thì H HCO3 CO2 H2O n 0,03mol;n 2 0,02mol;n 0,02mol H CO3 HCO3 nCO n n 2 0,01mol 2 H CO3 Câu 5: Cho m gam hỗn hợp bột X gồm Mg và Fe vào 800ml dung dịch chứa CuCl2 0,5M và HCl 1M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam hỗn hợp Y gồm hai kim loại. Khối lượng của Mg trong m gam hỗn hợp X là: A. 12,0g B. 7,2g C. 14,4g D. 13,8g Giải: Câu 13: Cho biết sản phẩm chính của phản ứng khử nước của (CH3)2CHCH(OH) CH2 CH3 ? A. 2 - metylpent-1-en B. 3 - metylpent-1-en C. 2 - metylpent-2-en D. 4 - metylpent-2-en Câu 14: Ứng với công thức phân tử C7H18O có bao nhiêu đồng phân phenol ? A. 2B. 3 C. 4 D. 5 Câu 15: Este vinyl axetat có công thức là A. CH3COOCH=CH2. B. CH3COOCH3. C. CH2=CHCOOCH3. D. HCOOCH3. Câu 16: Hợp chất hữu cơ mạch hở X có công thức phân tử C6H10O4. Thủy phân X tạo ra hai ancol đơn chức có số nguyên tử cacbon trong phân tử gấp đôi nhau. Công thức của X là: A. CH3OCO–CH2–COOC2H5. B. C2H5OCO–COOCH3. C. CH3OCO–COOC3H7. D. CH3OCO–CH2–CH2–COOC2H5. Câu 17: Cho ancol X tác dụng với axit Y thu được este Z. Làm bay hơi 4,3 gam Z thu được thể tích hơi bằng thể tích của 1,6 gam oxi ở cùng điều kiện nhiệt độ, áp suất. Biết MX>My. Công thức của Z là: A. CH3COOCH=CH2 B. CH2=CH-COOCH3 C. HCOOCH=CH-CH3 D. HCOOCH2CH=CH2. Câu 18: Hỗn hợp E gồm X, Y là hai axit đồng đẳng kế tiếp; Z,T là 2 este (đều hai chức, mạch hở; Y và Z là đồng phân của nhau; MT – MZ = 14). Đốt cháy hoàn toàn 12,84 gam E cần vừa đủ 0,37 mol O2, thu được CO2 và H2O. Mặt khác, cho 12,84 gam E phản ứng vừa đủ với 220 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được hỗn hợp muối khan G của các axit cacboxylic và 2,8 gam hỗn hợp 3 ancol có cùng số mol. Khối lượng muối của axit có phân tử khối lớn nhất trong G là A. 6,48 gam. B. 4,86 gam. C. 2,68 gam. D. 3,24 gam. Giải nCO2 = x và nH2O = y Bảo toàn khối lượng : 44x + 18y = 12,84 + 0,37.32 = 24,68 Bảo toàn oxi : 2x + y = 0,22.2 + 0,37.2 = 1,18 x = 0,43 và y = 0,32 nE = 0,44/4 = 0,11 = nCO2 – nH2O X,Y,Z,T đều 2 chức, no, mạch hở Số C TB = 0,43/0,11 = 3,9 X : C3H4O4 ; Y và Z : C4H6O4 ; T : C5H8O4 CTCT của Z : HCOO-CH2-CH2-OOCH (a mol) và T : CH3OOC-COO-C2H5 (a mol)
File đính kèm:
 de_thi_thu_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2018_2019_truon.docx
de_thi_thu_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2018_2019_truon.docx NV_LINH_CẤU TRÚC VA ĐỀ THI THỬ THPT QUỐC GIA NĂM 2018.pdf
NV_LINH_CẤU TRÚC VA ĐỀ THI THỬ THPT QUỐC GIA NĂM 2018.pdf

