Đề minh họa THPT Quốc gia năm 2018 môn Hóa học - Trường THPT Trần Quốc Tuấn (Có ma trận + đáp án)
Bạn đang xem tài liệu "Đề minh họa THPT Quốc gia năm 2018 môn Hóa học - Trường THPT Trần Quốc Tuấn (Có ma trận + đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề minh họa THPT Quốc gia năm 2018 môn Hóa học - Trường THPT Trần Quốc Tuấn (Có ma trận + đáp án)
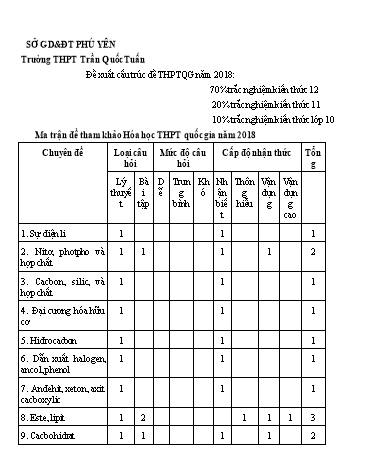
SỞ GD&ĐT PHÚ YÊN Trường THPT Trần Quốc Tuấn Đề xuất cấu trúc đề THPTQG năm 2018: 70% trắc nghiệm kiến thức 12 20% trắc nghiệm kiến thức 11 10% trắc nghiệm kiến thức lớp 10 Ma trận đề tham khảo Hóa học THPT quốc gia năm 2018 Chuyên đề Loại câu Mức độ câu Cấp độ nhận thức Tổn hỏi hỏi g Lý Bà D Trun Kh Nh Thôn Vận Vận thuyế i ễ g ó ận g dụn dụn t tập bình biế hiểu g g t cao 1. Sự điện li 1 1 1 2. Nitơ, photpho và 1 1 1 1 2 hợp chất 3. Cacbon, silic, và 1 1 1 hợp chất 4. Đại cương hóa hữu 1 1 1 cơ 5. Hiđrocacbon 1 1 1 6. Dẫn xuất halogen, 1 1 1 ancol, phenol 7. Anđehit, xeton, axit 1 1 1 cacboxylic 8. Este, lipit 1 2 1 1 1 3 9. Cacbohidrat 1 1 1 1 2 SỞ GD-ĐT PHÚ YÊN ĐỀ MINH HỌA THPT QUỐC GIA. NĂM 2018 TRƯỜNG THPT TRẦN QUỐC TUẤN Môn: KHOA HỌC TỰ NHIÊN - HÓA HỌC TỔ : HÓA Thời gian: 50 phút, không kể thời gian ------ phát đề Câu 1: Nguyên tử M có phân lớp mức năng lượng cao nhất là 3d 7. Tổng số electron của nguyên tử M là: A. 24 B. 25 C. 27 D. 29 Câu 2: Loại phản ứng hoá học nào sau đây luôn luôn là phản ứng oxi hoá-khử ? A. Phản ứng hoá hợp B. Phản ứng phân huỷ C. Phản ứng thế D. Phản ứng trao đổi Câu 3: Chọn dãy gồm các chất đều tác dụng được với dung dịch HCl? A. Fe2O3; KMnO4; C B. Fe; CuO; Ba(OH)2 C. CaCO3 ; H2SO4 ; Mg(OH)2 D. AgNO3 ; MgCO3; BaSO4 Câu 4: Oxi có thể thu được từ phản ứng nhiệt phân chất nào dưới đây ? A. CaCO3 B. KMnO4 C. (NH4)2SO4 D. NaHCO3 Câu 5: Các ion nào sau đây có thể cùng tồn tại trong một dung dịch? 2+ - + - 2+ + - A. Cu , Cl , Na , OH , NO3 B. Fe , K , OH , NH4 2 - 3+ 2+ - + 2+ C. NH4 , CO3 , HCO3 , OH , Al D. Cu , Cl , Na , Fe , NO3 . Câu 6: Ảnh hưởng của nhóm -OH đến gốc C6 H5- trong phân tử phenol thể hiện qua phản ứng giữa phenol với A. Na kim loại. B. H2 (Ni, nung nóng). C. dung dịch NaOH. D. nước Br2. Câu 7: Khi nhiệt phân AgNO3 thu được những sản phẩm nào? A. Ag, NO2, O2. B.Ag, NO,O2. C.Ag2O, NO2, O2. D.Ag2O, NO, O2. (5)Phản ứng thủy phân chất béo trong môi trường bazơ là phản ứng este hóa. Số phát biêu đúng là: A. (1),(2),(3),(5). B. (2),(3),(4),(5). C. (2),(3),(4). D.(1),(2),(4),(5). Câu 15: Công thức cấu tạo dạng mạch hở của glucozơ là A. CH2OH(CHOH)4CHO \ B. CH2OH(CHOH)3COCH2OH C. [C6H7O2(OH)3]n D. CH2OH(CHOH)4CH2OH Câu 16: Lysin là một aminoaxit có công thức cấu tạo sau: H2N-[CH2]4-CH(NH2)COOH Khi nhúng quỳ tím vào dung dịch Lysin, màu của quỳ tím A. không đổi. B. chuyển thành màu xanh. C. chuyển thành màu đỏ( hồng). D. chuyển thành màu xanh tím. Câu 17: Cho các chất metylamin, anilin, glyxin, axit glutamic. Số hợp chất hữu cơ no, đơn chức và có khả năng tác dụng với dung dịch HCl là A. 1B. 3C. 4D. 2 Câu 18:Trong số các loại tơ sau: tơ tằm, tơ visco, tơ nilon-6,6, tơ axetat, tơ capron, tơ enang, những loại tơ nào thuộc loại tơ nhân tạo? A. Tơ visco và tơ axetat. B. Tơ tằm và tơ enang. C. Tơ nilon-6,6 và tơ capron. D. Tơ visco và tơ nilon-6,6. Câu 19: Hai chất nào sau đây đều tham gia phản ứng trùng hợp tạo ra polime? A. Vinyl clorua và caprolactam. B. Axit aminoaxetic và etilen. C. Etan và propilen. D. Buta-1,3-đien và alanin. Câu 20 : Khi làm thí nghiệm với H2SO4 đặc nóng thường sinh ra khí SO2. Để hạn chế khí SO2 thoát ra gây ô nhiễm môi trường, người ta thường nút ống nghiệm bằng bông tẩm dung dịch A. muối ăn. B. Ancol. C. giấm ăn. D. kiềm. Câu 21: Phản ứng hóa học viết không đúng là A. CH3COOH + NaOH CH3COONa + H2O Câu 28: Cho dãy các chất: Cr(OH)3, Al2(SO4)3, Mg(OH)2, Zn(OH)2, MgO, CrO3. Số chất trong dãy có tính chất lưỡng tính là A. 5. B. 2. C. 3. D. 4. Câu 29: X, Y là hai este no, đơn chức, hở, thuộc cùng dãy đồng đẳng liên tiếp và đều được tạo thành từ một ancol Z. Đốt cháy hết m gam hỗn hợp H gồm X, Y, Z trong oxi, thu được 62,48g CO2 và 39,96g H2O. Mặt khác, m gam H tác dụng vừa đủ với 100 ml dung dịch NaOH 1,8M, cô cạn dung dịch sau phản ứng thu được a gam muối A; b gam muối B. Biết M A < MB. Tỉ lệ a : b có giá trị là: A. 1,094 B. 1,068 C. 0,914 D. 1,071 Định hướng tư duy giải CO2 :1,42 C3H6O2 : 0,1 Ta có: n Z 0,8 CH3OH CX,Y 3,44 H2O : 2,22 C4H8O2 : 0,08 a m 0,1.82 CH3COONa 1,068 b m 0,08.96 C2H5COONa Câu 30: Cho 0,2 mol alanin tác dụng với 200 ml dung dịch HCl thu được dung dịch X có chứa 28,75 gam chất tan. Hãy cho biết cần bao nhiêu ml dung dịch NaOH 1M để phản ứng vừa đủ với các chất trong dung dịch X? A. 100 ml B. 400 ml C. 500 ml D. 300 ml Câu 31:Cho m gam 3 kim loại Fe, Al, Cu vào một bình kín chứa 0,9 mol oxi. Nung nóng bình 1 thời gian cho đến khi số mol O2 trong bình chỉ còn 0,865 mol và chất rắn trong bình có khối lượng 2,12 gam. Giá trị m đã dùng là: A. 1,2 gam. B. 0,2 gam. C. 0,1 gam. D. 1,0 gam. Câu 32: Hòa tan hoàn toàn 1,94 gam hỗn hợp X chứa Na, K, Ca và Al trong nước dư thu được 1,12 lít khí (đktc) và dung dịch Y có chứa 2,92 gam chất tan. Phần trăm khối lượng của Al có trong X là ? A. 27,84% B. 34,79% C. 20,88% D. 13,92% Định hướng tư duy giải Kimloai :1,94(gam) 17a 32b 0,98 Ta có: nH 0,05 2,92 OH : a 2 a b 3b 0,05.2 O2 : b 0,02.27 a b 0,02 %Al 27,84% 1,94 Chọn đáp án C Quy E về C2H3NO, CH2, H2O. Bảo toàn nguyên tố Natri: nC2H3NO = nC2H4NO2Na = 2nNa2CO3 = 0,44 mol. Lại có: nO2 = 2,25.nC2H4NO2Na + 1,5.nCH2 ⇒ nCH2 = 0,11 mol. ⇒ nH2O = (28,42 - 0,44 × 57 - 0,11 × 14) ÷ 18 = 0,1 mol. ► Dễ thấy X là Gly2 || số mắt xích trung bình = 4,4. Lại có hexapeptit chứa ít nhất 12C ⇒ Z là pentapeptit. ● Dễ thấy Z là Gly4Ala ⇒ Y phải chứa Val ⇒ Y là GlyVal. Đặt nX = x; nY = y; nZ = z ⇒ nC2H3NO = 2x + 2y + 5z = 0,44. nH2O = x + y + z = 0,1 mol; nCH2 = 3y + z = 0,11 mol. ||⇒ Giải hệ có: x = y = 0,01 mol; z = 0,08 mol. ► %mX = 0,01 × 132 ÷ 28,42 × 100% = 4,64% ⇒ chọn C. Câu 36: Cho m gam hỗn hợp A gồm FexOy, Fe và Cu tác dụng hết với 200 gam dung dịch chứa HCl 32,85% và HNO3 9,45%, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m+60,24) gam chất tan. Cho a gam Mg vào dung dịch X, kết thúc các phản ứng thu được (m – 6,04) gam chất rắn và thấy thoát ra hỗn hợp khí Y gồm hai khí trong đó có một khí hóa nâu trong không khí, tỉ khối của Y so với He bằng 4,7. Giá trị của a gần nhất với giá trị nào sau đây ? A. 21,0. B. 23,0. C. 22,0. D. 24,0. Định hướng tư duy giải nHCl 1,8(mol) Ta có: n 0,3(mol) HNO3 BTKL m 1,8.36,5 0,3.63 m 60,24 0,26.30 18n H2O 0,92.2 0,26.4 n 0,92(mol) n trong A 0,4(mol) mTrong A m 6,4 H2O O 2 Fe,Cu Vậy trong (m – 6,04) có mMg 6,4 6,04 0,36(gam) Mg2 : x Dung dịch sau cùng chứa NH4 : y 2x y 1,8 Cl :1,8 NO :3z H Y 0,26 3z.4 2z.2 10y 10y 16z 0,26 H2 : 2z A. 2,1. B. 2,8. C. 2,4. D. 2,5. Định hướng tư duy giải 0,21.2 Nhìn vào đồ thị ta thấy ngay n 0,21 n 3 0,14 BaSO4 Al 3 n 0,07 BTNT.Ba n 0,21 0,07 0,28 V 2,8 Ba(AlO2 )2 Ba(OH)2 Câu 39: Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít H2 (đktc). Cho 3,2 lít dung dịch HCl 0,75M vào dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là A. 10,4. B. 27,3. C. 54,6. D. 23,4. Định hướng tư duy giải n 1,05(mol) n 0,35 O Al2O3 AlO2 : 0,7 Ta có: H:2,4 m 0,3.78 23,4 n 0,6 n 1,2 OH : 0,5 H2 OH Cách 2: Dùng điền số điện tích cho Cl- n 2,4 Cl Dung dịch cuối cùng chứa n 1,2 m (0,7 0,4).78 23,4 BTDT 3 Al : 0,4 Câu 40. Hòa tan hoàn toàn 23,76 gam hỗn hợp gồm Cu, FeCl2 và Fe(NO3)2 vào 400 ml dung dịch HCl 1M thu được dung dịch X. Cho lượng dư dung dịch AgNO3 dư vào X, thấy lượng AgNO3 phản ứng là 98,6 gam, thu được m gam kết tủa và thoát ra 0,448 lít khí (ở đktc). Các phản ứng xảy ra hoàn toàn và khí NO là sản phẩm khử duy nhất của N+5 trong cả quá trình. Giá trị của m gần nhất với giá trị nào sau đây? A. 82. B. 80. C. 84. D. 86. Chọn đáp án A + – Do Y tác dụng AgNO3 sinh ra NO ⇒ trong Y có chứa H và NO3 hết. + – + 4H + NO3 + 3e → NO + 2H2O ⇒ ở phản ứng đầu, nH = 0,4 – 0,02 × 4 = 0,32 mol. – ⇒ nNO3 = 0,32 ÷ 4 = 0,08 mol ⇒ nFe(NO3)2 = 0,04 mol. Đặt nFeCl2 = x mol; nCu = y mol. mX = 127x + 64y + 0,04 × 180 = 23,76 gam. Bảo toàn nguyên tố Clo : nAgCl = 2x + 0,4 mol. Bảo toàn nguyên tố Ag : nAg = 0,58 – (2x + 0,4) = 0,18 – 2x mol.
File đính kèm:
 de_minh_hoa_thpt_quoc_gia_nam_2018_mon_hoa_hoc_truong_thpt_t.docx
de_minh_hoa_thpt_quoc_gia_nam_2018_mon_hoa_hoc_truong_thpt_t.docx

