Đề minh họa THPT Quốc gia môn Hóa học - Năm học 2019-2020 - Trường THPT Lê Lợi (Có đáp án)
Bạn đang xem tài liệu "Đề minh họa THPT Quốc gia môn Hóa học - Năm học 2019-2020 - Trường THPT Lê Lợi (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề minh họa THPT Quốc gia môn Hóa học - Năm học 2019-2020 - Trường THPT Lê Lợi (Có đáp án)
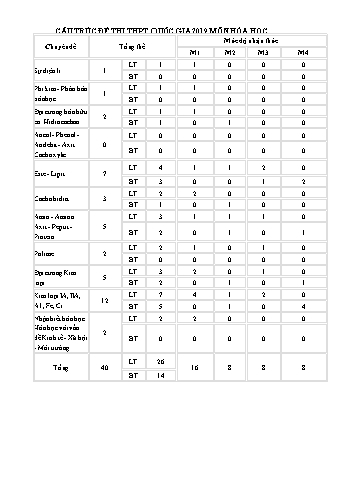
CẤU TRÚC ĐỀ THI THPT QUỐC GIA 2019 MÔN HÓA HỌC Mức độ nhận thức Chuyên đề Tổng thể M1 M2 M3 M4 LT 1 1 0 0 0 Sự điện li 1 BT 0 0 0 0 0 Phi kim - Phân bón LT 1 1 0 0 0 1 hóa học BT 0 0 0 0 0 Đại cương hóa hữu LT 1 1 0 0 0 2 cơ. Hidrocacbon BT 1 0 1 0 0 Ancol - Phenol - LT 0 0 0 0 0 Andehit - Axit 0 Cacboxylic BT 0 0 0 0 0 LT 4 1 1 2 0 Este - Lipit 7 BT 3 0 0 1 2 LT 2 2 0 0 0 Cacbohidrat 3 BT 1 0 1 0 0 Amin - Amino LT 3 1 1 1 0 Axit - Peptit - 5 BT 2 0 1 0 1 Protein LT 2 1 0 1 0 Polime 2 BT 0 0 0 0 0 Đại cương Kim LT 3 2 0 1 0 5 loại BT 2 0 1 0 1 Kim loại IA, IIA, LT 7 4 1 2 0 12 A1, Fe, Cr BT 5 0 1 0 4 Nhận biết hóa học. LT 2 2 0 0 0 Hóa học với vấn 2 đề Kinh tế - Xã hội BT 0 0 0 0 0 - Môi trường LT 26 Tổng 40 16 8 8 8 BT 14 Câu 16. Polime nào sau đây thuộc loại tơ poliamit? A. Tơ nitron.B. Tơ axetatC. Tơ visco.D. Tơ nilon - 6,6 Câu 17. Chất bị thủy phân trong môi trường kiềm là A. SaccarozơB. Polietilen.C. Gly-Ala-GlyD. Tinh bột Câu 18. Cho 250ml dung dịch glucozơ phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 5,4 gam Ag. Nồng độ mol của dung dịch glucozơ đã dùng là A. 0,20MB. 0,50MC. 0,10M.D. 0,25M. Câu 19. Trường hợp nào sau đây, kim loại bị ăn mòn điện hóa học A. Nhúng thanh sắt nguyên chất vào dung dịch CuSO4. B. Đốt sợi dây đồng trong bình đựng khí clo. C. Nhúng sợi dây bạc nguyên chất vào dung dịch HNO3 loãng. D. Nhúng thanh sắt nguyên chất vào dung dịch H2SO4 loãng. Câu 20. Cho dãy các chất: HCHO, CH3COOH, CH3COOC2H5, HCOOH, C2H5OH, HCOOCH3. Số chất trong dãy tham gia phản ứng tráng gương là A. 4.B. 5.C. 6.D. 3. + Câu 21. Cho các chất và các dung dịch sau: K2O; dung dịch HNO3; dung dịch KMnO4/H , dung dịch AgNO3;dung dịch NaNO3; dung dịch nước Brom; dung dịch NaOH; dung dịch CH3NH2; dung dịch H2S. Số chất và dung dịch phản ứng được với dung dịch FeCl2 mà tạo thành sản phẩm không có chất kết tủa là A. 2B. 3C. 4D. 5. Câu 22. Phương pháp điện phân dung dịch dùng để điều chế kim loại A. Na, NiB. Cu, Ag C. Al, CuD. Ca, Fe Câu 23. Hợp chất X có công thức cấu tạo: CH3CH2COOCH3. Tên gọi của X là: A. Propyl axetat.B. Metyl axetat.C. Metyl propionatD. Etyl axetat. Câu 24. Chất có khả năng tạo phức màu xanh lam với Cu(OH)2 ở nhiệt độ thường là A. Phenol.B. EtanolC. Etyl axetatD. Saccarozơ Câu 25. Muối nào sau đây dễ bị nhiệt phân? A. Na2CO3.B. NaNO 2 C. NaCl.D. NH 4HCO3. Câu 26. Công thức của crom (VI) oxit là A. CrO.B. CrO 3.C. Cr 2O3.D. Cr 2O6. Câu 27. Hình vẽ sau đây mô tả thí nghiệm điều chế khí Y từ hỗn hợp rắn gồm CaC2 và Al4C3 Khí Y là A. C2H4. B. C2H6. C. CH4. D. C2H2 Câu 28. Este X được điều chế từ aminoaxit A và ancol B. Hóa hơi 2,06 gam X hoàn toàn chiếm thể tích bằng thể tích của 0,56 gam nito ở cùng điều kiện nhiệt độ, áp xuất. Biết rằng từ B có thể điều chế cao su Buna bằng 2 giai đoạn. Hợp chất X có công thức cấu tạo là A. H2NCH2CH2COOCH3.B. NH 2COOCH2CH2CH3. C. H2NCH2COOCH2CH3.D. CH 3NHCOOCH2CH3. Câu 29. Thực hiện các thí nghiệm sau: (a) Cho dung dịch Ba(OH)2 tới dư vào dung dịch FeCl2. (b) Cho dung dịch KHSO4 vào dung dịch BaCl2. (c) Cho dung dịch Na2S vào dung dịch Fe2(SO4)3. (2) Saccarozo là một polisaccarit, không màu, thủy phân tạo glucozo và fructozo (3) Glucozo tác dụng với Hiđro (xúc tác Ni,đun nóng) tạo sobitol (4) Trong môi trường axit, glucozo và fructozo có thể chuyển hóa qua lại lẫn nhau. (5) Trùng hợp isopren thu được cao su thiên nhiên.Số mệnh đề đúng là: A. 5B. 4C. 3D. 2 Câu 37. Hỗn hợp E gồm muối vô cơ X (CH8N2O3) và đipeptit Y (C4H8N2O3). Cho E tác dụng với dung dịch NaOH đun nóng, thu được khí Z. Cho E tác dụng với dung dịch HCl dư, thu được khí T và chất hữu cơ Q. Nhận định nào sau đây sai? A. Chất Z là NH3 và chất T là CO2.B. Chất X là (NH 4)2CO3. C. Chất Y là H2NCH2CONHCH2COOH.D. Chất Q là H 2NCH2COOH. Câu 38. Dẫn luồng khí CO đi qua hỗn hợp gồm CuO và Fe 2O3 nung nóng, sau một thời gian thu được chất rắn X và khí Y. Cho hấp thụ hoàn toàn vào dung dịch Ba(OH) 2 dư, thu được 29,55 gam kết tủa. Chất rắn X phản ứng với dung dịch HNO3 dư thu được V lít khí NO (sản phẩm khử duy nhất và ở đktc). Giá trị của m là A. 4,48. B. 2,24. C. 6,72. D. 3,36. Câu 39. Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO 3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO 3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N 2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO 3, thu được 0,448 lít NO (đktc) là sản phẩm khử duy nhất và m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây? A. 413. B. 415. C. 411. D. 414. Câu 40.Sục từ từ khí CO2 đến dư vào dung dịch X (chứa m (gam) NaOH và a mol Ca(OH)2). Kết quả thí nghiệm được biểu diễn trên đồ thị sau: Giá trị của m và a lần lượt là: A. 48 và 1,2. B. 36 và 1,2. C. 48 và 0,8. D. 36 và 0,8. III. ĐÁP ÁN THAM KHẢO: PHẦN ĐÁP ÁN 1D 2C 3C 4D 5C 6D 7D 8A 9B 10A 11A 12D 13A 14D 15A 16D 17C 18C 19A 20D 21C 22B 23C 24D 25D 26B 27C 28C 29B 30A 31D 32A 33B 34A 35C 36D 37D 38B 39D 40C HƯỚNG DẪN GIẢI CHI TIẾT Câu 30:Chọn A. n = 0,15 tính đc n 0,1mol n 2 = 0,1 mol H 2 Na Ba n 2 0,125mol n 2 0,1mol Cu SO 4 n OH = 0,05mol m m m = 25,75 gam BaSO 4 Cu(OH )2 Câu 32: Chọn A. x số mol chất béo BT O: 6x + 4,83 .2 = 3,42 . 2 + 3,18 x = 0,06 mol BTKL : mcbeo = 53,16 Gam
File đính kèm:
 de_minh_hoa_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2019_2020_truo.doc
de_minh_hoa_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2019_2020_truo.doc

