Đề minh họa THPT Quốc gia 2018 môn Hóa học - Trường THPT Tôn Đức Thắng (Có đáp án)
Bạn đang xem tài liệu "Đề minh họa THPT Quốc gia 2018 môn Hóa học - Trường THPT Tôn Đức Thắng (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề minh họa THPT Quốc gia 2018 môn Hóa học - Trường THPT Tôn Đức Thắng (Có đáp án)
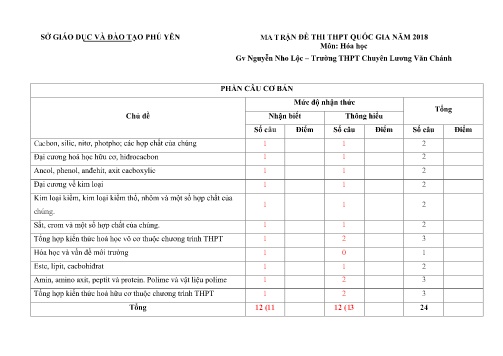
SỞ GIÁO DỤC VÀ ĐÀO TẠO PHÚ YÊN MA TRẬN ĐỀ THI THPT QUỐC GIA NĂM 2018 Môn: Hóa học Gv Nguyễn Nho Lộc – Trƣờng THPT Chuyên Lƣơng Văn Chánh PHẦN CÂU CƠ BẢN Mức độ nhận thức Tổng Chủ đề Nhận biết Thông hiểu Số câu Điểm Số câu Điểm Số câu Điểm Cacbon, silic, nitơ, photpho; các hợp chất của chúng 1 1 2 Đại cương hoá học hữu cơ, hiđrocacbon 1 1 2 Ancol, phenol, anđehit, axit cacboxylic 1 1 2 Đại cương về kim loại 1 1 2 Kim loại kiềm, kim loại kiềm thổ, nhôm và một số hợp chất của 1 1 2 chúng. Sắt, crom và một số hợp chất của chúng. 1 1 2 Tổng hợp kiến thức hoá học vô cơ thuộc chương trình THPT 1 2 3 Hóa học và vấn đề môi trường 1 0 1 Este, lipit, cacbohiđrat 1 1 2 Amin, amino axit, peptit và protein. Polime và vật liệu polime 1 2 3 Tổng hợp kiến thức hoá hữu cơ thuộc chương trình THPT 1 2 3 Tổng 12 (11 12 (13 24 Câu 14: Hợp chất X khi đun nhẹ với dd AgNO3/NH3 dư được sản phẩm Y. Cho Y tác dụng với dd HCl hoặc dd NaOH thì sản phẩm khí thu được đều là chất khí vô cơ. Vậy X là chất nào sau đây thì phù hợp. A. HCHO B. HCOOH C. HCOONH4 D. CH3COOH Câu 15: Tiến hành bốn thí nghiệm sau: - Thí nghiệm 1: Nhúng thanh Fe vào dung dịch FeCl3; - Thí nghiệm 2: Nhúng thanh Fe vào dung dịch CuSO4; - Thí nghiệm 3: Nhúng thanh Cu vào dung dịch FeCl3; - Thí nghiệm 4: Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl. Số trường hợp xuất hiện ăn mòn điện hoá là: A. 1. B. 2. C. 4. D. 3. Câu 16: Cho từ từ dung dịch NH3 đến dư vào dung dịch AlCl3 thì có hiện tượng nào sau đây ? A. Dung dịch vẫn trong suốt B. Xuất hiện kết tủa keo, kết tủa tăng đến cực đại rồi tan dần đến hết C. Xuất hiện kết tủa và kết tủa nay không tan D. Xuất hiện kết tủa và có khí không mùi thoát ra Câu 17: Một loại quặng trong tự nhiên đã loại bỏ hết tạp chất. Hoà tan quặng này trong axit HNO3 thấy có khí màu nâu bay ra, dung dịch thu được cho tác dụng với dung dịch BaCl2 thấy có kết tủa trắng xuất hiện (không tan trong axit). Quặng đó là: A. Xiđêrit B. Manhetit C. Hematit D. Pirit Câu 18: Cho dung dịch FeCl2, ZnCl2 tác dụng với dung dịch NaOH dư, lấy kết tủa thu được nung khan trong không khí đến khối lượng không đổi, chất rắn thu được là A. FeO, ZnO B. Fe2O3, ZnO C. Fe2O3 D. FeO 2+ + 2+ 2+ - Câu 19: Một dung dịch có chứa các ion : Fe , K , Cu , Ba và NO 3. Hãy cho biết có thể sử dụng hoá chất nào sau đây để nhận biết sự có mặt của ion Fe2+ có trong dung dịch trên ? A. dung dịch NaOH B. dung dịch HCl C. dung dịch Na2CO3 D. dung dịch NH3 Câu 20: Dãy gồm các dung dịch đều tác dụng với Cu(OH)2 ở điều kiện thường là A. glucozơ, glixerol, ancol etylic. B. glucozơ, andehit fomic, natri axetat. C. glucozơ, glixerol, axit axetic. D. glucozơ, glixerol, natri axetat. Câu 21: Để phân biệt 3 dung dịch H2NCH2COOH, CH3COOH và C2H5NH2 chỉ cần dùng một thuốc thử là A. dung dịch NaOH. B. dung dịch HCl. C. natri kim loại. D. quỳ tím. Câu 22: Cho các chất sau : 1. CH3CH(NH2)COOH 2. HOOC-CH2-CH2-COOH 3. HO-CH2-COOH 4. HCHO và C6H5OH 5. HO-CH2-CH2-OH và p-C6H4(COOH)2 6. H2N[CH2]6NH2 và HOOC(CH2)4COOH Các trường hợp có thể tham gia phản ứng trùng ngưng là A. 1, 3, 4, 5, 6. B. 1, 2, 3, 4, 5, 6. C. 1, 6. D. 1, 3, 5, 6. Câu 23. Cho dãy các chất: HCHO, CH3COOH, CH3COOC2H5, HCOOH, C2H5OH, HCOOCH3. Số chất trong dãy tham gia phản ứng tráng bạc là: A. 6. B. 4. C. 5. D. 3. Câu 24: Cho X, Y, Z, T là các chất không theo thứ tự : CH3NH2, NH3, C6H5OH (phenol), C6H5NH2 (anilin) và pH các dung dịch có cùng CM được ghi trong bảng sau. Chất X Y Z T pH (dungdịch nồng độ 6,48 7,82 10,8 10,12 0,001M) 1 C. (CH3COO)3C3H5 D. (C17H35COO)3C3H5 Câu 34: Cho 0,7 mol hỗn hợp T gồm hai peptit mạch hở là X (x mol) và Y (y mol), đều tạo bởi glyxin và alanin. Đun nóng 0,7 mol T trong lượng dư dung dịch NaOH thì có 3,8 mol NaOH phản ứng và thu được dung dịch chứa m gam muối. Mặt khác, nếu đốt cháy hoàn toàn x mol X hoặc y mol Y thì đều thu được cùng số mol CO2. Biết tổng số nguyên tử oxi trong hai phân tử X và Y là 13, trong X và Y đều có số liên kết peptit không nhỏ hơn 4. Giá trị của m là A. 396,6 B. 340,8 C. 409,2 D. 399,4 Câu 35: Hỗn hợp X gồm 2 chất có công thức phân tử là C3H12N2O3 và C2H8N2O3. Cho 3,40 gam X phản ứng vừa đủ với dung dịch NaOH (đun nóng), thu được dung dịch Y chỉ gồm các chất vô cơ và 0,04 mol hỗn hợp 2 chất hữu cơ đơn chức (đều làm xanh giấy quỳ tím ẩm). Cô cạn Y, thu được m gam muối khan. Giá trị của m là: A. 3,12 B. 2,76 C. 3,36 D. 2,97 Câu 36: Hỗn hợp X gồm hai chất hữu cơ no , mạch hở (đều chứa C, H, O), trong phân tử mỗi chất có hai nhóm chức trong số các nhóm –OH, -CHO, -COOH. Cho m gam X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 4,05 gam Ag và 1,86 gam một muối amoni hữu cơ. Cho toàn bộ lượng muối amoni hữu cơ này vào dung dịch NaOH (dư, đun nóng), thu được 0,02 mol NH3. Giá trị của m là: A. 1,24 B. 2,98 C. 1,22 D. 1,50 Câu 37: Dung dịch X có chứa AgNO3 và Cu(NO3)2 có cùng nồng độ. Thêm một lượng hỗn hợp gồm 0,03 mol Al và 0,05 mol Fe vào 100 ml dung dịch X cho tới khi phản ứng kết thúc thu được chất rắn Y gồm 3 kim loại. Cho Y vào HCl dư giải phóng 0,07 gam khí. Nồng độ mol/lít của hai muối là A. 0,30. B. 0,40 . C. 0,63. D. 0,42. Câu 38: hòa tan hoàn toàn 21,5 gam hỗn hợp X gồm Al, Zn, FeO và Cu(NO3)2 cần dùng hết 430 ml dung dịch H2SO4 1M thu được hỗn hợp khí Y (đktc) gồm 0,06 mol NO và 0,13 mol H2, đồng thời thu được dung dịch Z chỉ chứa các muối sunfat trung hòa. Cô cạn dung dịch Z thu được 56,9 gam muối khan. Thành phần phần trăm khối lượng của Al trong hỗn hợp X có giá trị gần nhất là: A. 25.5% B. 18,5% C. 20,5% D. 22,5% Câu 39: X, Y, Z là 3 este đều đơn chức, mạch hở (Trong đó Y và Z không no có một liên kết C=C) đốt cháy 21,62 gam hỗn hợp E chứa X, Y, Z với oxi vừa đủ, sản phẩm cháy dẫn qua dung dịch Ca(OH)2 dư thấy khối lượng dung dịch giảm 34,5 gam so với trước phản ứng. Mặt khác, đung nóng 21,62 gam E với 300 ml dung dịch NaOH 1M ( vừa đủ) thu được hỗn hợp F chỉ chứa 2 muối và hỗn hợp gồm hai ancol kế tiếp thuộc cùng dãy đồng đẳng. % khối lượng của este có khối lượng phân tử lớn nhất trong E là A. 21.09% B. 15,81% C. 26,36% D. 31,64% Câu 40: Hỗn hợp X gồm 3 este đơn chức, tạo thành từ cùng một ancol Y với 3 axit cacboxylic (phân tử chỉ có nhóm -COOH); trong đó, có hai axit no là đồng đẳng kế tiếp nhau và một axit không no (có đồng phân hình học, chứa một liên kết đôi C=C trong phân tử). Thủy phân hoàn toàn 5,88 gam X bằng dung dịch NaOH, thu được hỗn hợp muối và m gam ancol Y. Cho m gam Y vào bình đựng Na dư, sau phản ứng thu được 896 ml khí (đktc) và khối lượng bình tăng 2,48 gam. Mặt khác, nếu đốt cháy hoàn toàn 5,88 gam X thì thu được CO2 và 3,96 gam H2O. Phần trăm khối lượng của este không no trong X là A. 38,76% B. 40,82% C. 34,01% D. 29,25% A.Al2O3 ;Cu;Fe;Mg B.Al2O3;Cu;Fe;MgO C.Al;Fe;Cu;MgO D.Al;Cu;Fe;Mg Câu 13: Cho các chất : C6H5OH (X) ; C6H5CH2OH (Y) ; HOC6H4OH (Z) ; C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là: A. Y, T. B. X, Z, T. C. X, Z. D. Y, Z. Câu 14: Hợp chất X khi đun nhẹ với dd AgNO3/NH3 dư được sản phẩm Y. Cho Y tác dụng với dd HCl hoặc dd NaOH thì sản phẩm khí thu được đều là chất khí vô cơ. Vậy X là chất nào sau đây thì phù hợp. A. HCHO B. HCOOH C. HCOONH4 D. CH3COOH Câu 15: Tiến hành bốn thí nghiệm sau: - Thí nghiệm 1: Nhúng thanh Fe vào dung dịch FeCl3; - Thí nghiệm 2: Nhúng thanh Fe vào dung dịch CuSO4; - Thí nghiệm 3: Nhúng thanh Cu vào dung dịch FeCl3; - Thí nghiệm 4: Cho thanh Fe tiếp xúc với thanh Cu rồi nhúng vào dung dịch HCl. Số trường hợp xuất hiện ăn mòn điện hoá là: A. 1. B. 2. C. 4. D. 3. Câu 16: Cho từ từ dung dịch NH3 đến dư vào dung dịch AlCl3 thì có hiện tượng nào sau đây ? A. Dung dịch vẫn trong suốt B. Xuất hiện kết tủa keo, kết tủa tăng đến cực đại rồi tan dần đến hết C. Xuất hiện kết tủa và kết tủa nay không tan D. Xuất hiện kết tủa và có khí không mùi thoát ra Câu 17: Một loại quặng trong tự nhiên đã loại bỏ hết tạp chất. Hoà tan quặng này trong axit HNO3 thấy có khí màu nâu bay ra, dung dịch thu được cho tác dụng với dung dịch BaCl2 thấy có kết tủa trắng xuất hiện (không tan trong axit). Quặng đó là: A. Xiđêrit B. Manhetit C. Hematit D. Pirit Câu 18: Cho dung dịch FeCl2, ZnCl2 tác dụng với dung dịch NaOH dư, lấy kết tủa thu được nung khan trong không khí đến khối lượng không đổi, chất rắn thu được là A. FeO, ZnO B. Fe2O3, ZnO C. Fe2O3 D. FeO 2+ + 2+ 2+ - Câu 19: Một dung dịch có chứa các ion : Fe , K , Cu , Ba và NO 3. Hãy cho biết có thể sử dụng hoá chất nào sau đây để nhận biết sự có mặt của ion Fe2+ có trong dung dịch trên ? A. dung dịch NaOH B. dung dịch HCl C. dung dịch Na2CO3 D. dung dịch NH3 Câu 20: Dãy gồm các dung dịch đều tác dụng với Cu(OH)2 ở điều kiện thường là A. glucozơ, glixerol, ancol etylic. B. glucozơ, andehit fomic, natri axetat. C. glucozơ, glixerol, axit axetic. D. glucozơ, glixerol, natri axetat. Câu 21: Để phân biệt 3 dung dịch H2NCH2COOH, CH3COOH và C2H5NH2 chỉ cần dùng một thuốc thử là A. dung dịch NaOH. B. dung dịch HCl. C. natri kim loại. D. quỳ tím. Câu 22: Cho các chất sau : 1. CH3CH(NH2)COOH 2. HOOC-CH2-CH2-COOH 3. HO-CH2-COOH 4. HCHO và C6H5OH 5. HO-CH2-CH2-OH và p-C6H4(COOH)2 6. H2N[CH2]6NH2 và HOOC(CH2)4COOH Các trường hợp có thể tham gia phản ứng trùng ngưng là A. 1, 3, 4, 5, 6. B. 1, 2, 3, 4, 5, 6. C. 1, 6. D. 1, 3, 5, 6. Câu 23. Cho dãy các chất: HCHO, CH3COOH, CH3COOC2H5, HCOOH, C2H5OH, HCOOCH3. Số chất trong dãy tham gia phản ứng tráng bạc là: Giá trị của x là A. 0,12 mol. B. 0,11 mol. C. 0,13 mol. D. 0,10 mol. Giải câu 29: Từ đồ thì suy ra: AD = 0,15; AE = CD = BE = 0,5 – 0,45 = 0,05. x = DE = AD – AE = 0,15 – 0,05 = 0,1 mol. Câu 30: Cho luồng khí CO đi qua một lượng quặng hematit ( chứa Fe2O3 ) thì thu được 300,8 gam hỗn hợp các chất rắn X và thoát ra hỗn hợp khí Y. Cho hấp thụ toàn bộ khí Y bằng dung dịch NaOH dư thấy khối lượng bình NaOH tăng thêm 52,8 gam. Đem chất rắn X hòa tan trong dung dịch HNO3 dư thu được 387,2 gam muối. Thành phần % khối lượng của Fe2O3 trong quặng là : A.80% B.60% C.50% D.40% Giải câu 30: mtăng = mCO2 = 52,8 gam => nO ( bị khử ) = nCO2 = 1,2 mol => Khối lượng của quặng = mX + mO = 300,8 +1,2.16 = 320 gam .BTNT Fe : nFe2O3 = ½ nFe(NO3)3 = 0,8 mol => % mFe2O3 = 0,8.160/320.100% = 40% Câu 31: Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10 %, thu được 2,24 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là: A. 101,68 gam B. 88,20 gam C. 101,48 gam D. 97,80 gam Giải câu 31: nH2 = nH2SO4 = 0,1 mol → m (dung dịch H2SO4) = 98 gam → m (dung dịch sau phản ứng) = 3,68 + 98 - 0,2 = 101,48 gam → đáp án C Câu 32:Sau một thời gian điện phân 200 ml dung dịch CuSO4 ( d = 1,25 g/ml) với điện cực graphit (than chì) thấy khối lượng dung dịch giảm 8 gam. Để làm kết tủa hết ion Cu2+ còn lại trong dung dịch sau điện phân cần dùng 100 ml dung dịch H2S 0,5 M. Nồng độ phần trăm của dung dịch CuSO4 ban đầu là: A. 12,8 % B. 9,6 % C. 10,6 % D. 11,8 % Giải câu 32: nH2S = 0,05 mol - Gọi x là số mol CuSO4 tham gia quá trình điện phân: CuSO4 + H2O → Cu + 1/2O2 + H2SO4 (1) → m (dung dịch giảm) = m Cu(catot) + m O2(anot) = 64x + 16x = 8 → x = 0,1 mol - CuSO4 + H2S → CuS + H2SO4 (2) → nH2S = nCuSO4 = 0,05 mol . Từ (1) và (2) → nCuSO4 (ban đầu) = 0,1 + 0,05 = 0,15 (mol) → C% = → đáp án B Bài 33: Một este A (không chứa chức nào khác) mạch hở được tạo ra từ 1 axit đơn chức và rượu no. Lấy 2,54 gam A đốt cháy hoàn toàn thu được 2,688 lít CO2 (đktc) và 1,26 gam H2O . 0,1 mol A phản ứng vừa đủ với 12 gam NaOH tạo ra muối và rượu. Đốt cháy toàn bộ lượng rượu này được 6,72 lít CO2 (đktc). Xác định CTPT, CTCT của A A. (C2H5COO)3C3H5 B. (C2H3COO)3C3H5 C. (CH3COO)3C3H5 D. (C17H35COO)3C3H5 Giải câu 33: nA:nNaOH = 1:3 (RCOO)3R’ + 3NaOH 3RCOONa + R’(OH)3
File đính kèm:
 de_minh_hoa_thpt_quoc_gia_2018_mon_hoa_hoc_truong_thpt_ton_d.pdf
de_minh_hoa_thpt_quoc_gia_2018_mon_hoa_hoc_truong_thpt_ton_d.pdf

