Đề minh họa thi THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Phạm Văn Đồng (Có đáp án)
Bạn đang xem tài liệu "Đề minh họa thi THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Phạm Văn Đồng (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề minh họa thi THPT Quốc gia môn Hóa học - Năm học 2018-2019 - Trường THPT Phạm Văn Đồng (Có đáp án)
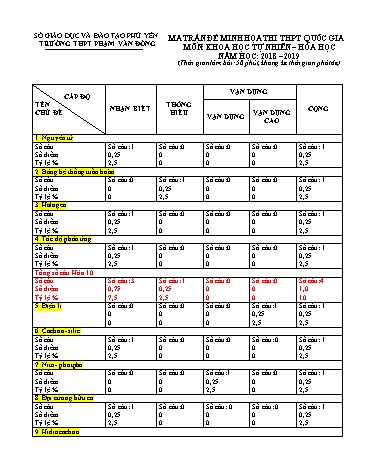
SỞ GIÁO DỤC VÀ ĐÀO TẠO PHÚ YÊN MA TRẬN ĐỀ MINH HỌA THI THPT QUỐC GIA TRƯỜNG THPT PHẠM VĂN ĐỒNG MÔN: KHOA HỌC TỰ NHIÊN – HÓA HỌC NĂM HỌC: 2018 – 2019 (Thời gian làm bài: 50 phút, không kể thời gian phát đề) VẬN DỤNG CẤP ĐỘ TÊN THÔNG NHẬN BIẾT VẬN DỤNG CỘNG CHỦ ĐỀ HIỂU VẬN DỤNG CAO 1. Nguyên tử Số câu Số câu: 1 Số câu:0 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0,25 0 0 0 0,25 Tỷ lệ % 2,5 0 0 0 2,5 2. Bảng hệ thống tuần hoàn Số câu Số câu:0 Số câu: 1 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0 0,25 0 0 0,25 Tỷ lệ % 0 2,5 0 0 2,5 3. Halogen Số câu Số câu: 1 Số câu:0 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0,25 0 0 0 0,25 Tỷ lệ % 2,5 0 0 0 2,5 4. Tốc độ phản ứng Số câu Số câu: 1 Số câu:0 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0,25 0 0 0 0,25 Tỷ lệ % 2,5 0 0 0 2,5 Tổng số câu Hóa 10 Số câu Số câu: 3 Số câu: 1 Số câu:0 Số câu:0 Số câu:4 Số điểm 0,75 0,25 0 0 1,0 Tỷ lệ % 7,5 2,5 0 0 10 5. Điện li Số câu:0 Số câu:0 Số câu:0 Số câu:1 Số câu: 1 0 0 0 0,25 0,25 0 0 0 2,5 2,5 6. Cacbon- silic Số câu Số câu: 1 Số câu:0 Số câu:0 Số câu: 0 Số câu: 1 Số điểm 0,25 0 0 0 0,25 Tỷ lệ % 2,5 0 0 0 2,5 7. Nito- photpho Số câu Số câu:0 Số câu:0 Số câu:1 Số câu:0 Số câu: 1 Số điểm 0 0 0,25 0 0,25 Tỷ lệ % 0 0 2,5 0 2,5 8. Đại cương hữu cơ Số câu Số câu: 1 Số câu:0 Số câu: 0 Số câu: 0 Số câu: 1 Số điểm 0,25 0 0 0 0,25 Tỷ lệ % 2,5 0 0 0 2,5 9. Hidrocacbon Số câu Số câu: 1 Số câu:1 Số câu: 1 Số câu: 1 Số câu: 4 Số điểm 0,25 0,25 0,25 0,25 1 Tỷ lệ % 2,5 2,5 2,5 2,5 10 20.Nhận biết các chất Số câu Số câu:0 Số câu:1 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0 0,25 0 0 0,25 Tỷ lệ % 0 2,5 0 0 2,5 21. Hóa học và vấn đề phát triển kinh tế, xã hội và ô nhiễm môi trường Số câu Số câu:0 Số câu:1 Số câu:0 Số câu:0 Số câu: 1 Số điểm 0 0,25 0 0 0,25 Tỷ lệ % 0 2,5 0 0 2,5 22. Tổng hợp vô cơ 12 Số câu Số câu: 2 Số câu:0 Số câu:1 Số câu:0 Số câu: 3 Số điểm 0,5 0 0,25 0 0,75 Tỷ lệ % 5 0 2,5 0 7,5 Tổng số câu Hóa 12 10 7 5 6 Số câu : 28 Tổng số điểm 2,5 1,75 1,25 1,5 7,0 Tỷ lệ % 25 17,5 12,5 15 70 Tổng cộng 16 9 7 8 Số câu 40 Tổng số điểm 4,0 2,25 1,75 2,0 Tỷ lệ % 40 22,5 17,5 20 Câu 14: Dãy gồm các dung dịch đều tham gia phản ứng tráng bạc là: A. Fructozơ, mantozơ, glixerol, anđehit axetic. B. Glucozơ, mantozơ, axit fomic, anđehit axetic. C. Glucozơ, glixerol, mantozơ, axit fomic. D. Glucozơ, fructozơ, mantozơ, saccarozơ. Câu 15: Kim loại không tác dụng với axit clohidric (HCl) là: A. AlB. ZnC. FeD. Ag Câu 16:Oxit dễ bị H2 khử ở nhiệt độ cao tạo thành kim loại là: A. Na2O B. CaO C. K2OD. CuO Mức độ hiểu gồm 09câu ( từ câu 17 đến câu 25) Câu 17: Nhúng 1 lá sắt vào các dung dịch : HCl, HNO 3đặc,nguội, CuSO4, FeCl2, ZnCl2, FeCl3. Số phản ứng hóa học xảy ra là: A. 2B. 3C. 4D. 5 Câu 18: Để điều chế kim loại Na người ta dùng phương pháp nào trong các phương pháp sau: (1) Điện phân nóng chảy NaCl; (2) Điện phân nóng chảy NaOH (3) Điện, phân dung dịch NaCl có màng ngăn; (4) Khử Na2O bằng H2 ở nhiệt độ cao A. (2),(3),(4) B. (1),(2),(4)C. (1),(3) D. (1),(2) Câu 19: Khi làm thí nghiệm tại lớp hoặc trong giờ thực hành hóa học, có một số khí thải độc hại cho sức khỏe khi tiến hành thí nghiệm HNO 3đặc (HNO3loãng) tác dụng với Cu. Để giảm thiểu các khí thải đó ta dùng cách nào sau đây? A. Dùng nút bông tẩm etanol hoặc sục ống dẫn khí vào chậu chứa etanol. B. Dùng nút bông tẩm giấm ăn hoặc sục ống dẫn khí vào chậu chứa giấm ăn. C. Dùng nút bông tẩm nước muối hoặc sục ống dẫn khí vào chậu chứa nước muối. D. Dùng nút bông tẩm dung dịch xút hoặc sục ống dẫn khí vào chậu chứa dd xút. Câu 20: Một nguyên tố A có cấu hình electron là 1s22s22p5. Công thức hợp chất của A với hiđro là: A. AH3 B. AH7 C. AH D. AH5 Câu 21: Cho sơ đồ phản ứng: +H2O men rîu men giÊm +Y Xenluloz¬ X Y Z o T . H+, to xt, t Công thức của T là: A. C2H5COOH.B. C 2H5COOCH3. C. CH3COOH.D. CH 3COOC2H5. Câu 22: Có các lọ hóa chất mất nhãn mỗi lọ đựng một trong các dung dịch sau: FeCl2, (NH4)2SO4 , FeCl3, CuCl2, AlCl3, NH4Cl. Chỉ dùng dung dịch NaOH lần lượt thêm vào từng dung dịch có thể nhận biết tối đa được mấy dung dịch trong số các dung dịch trên? A. 2 B. 3 C. 6 D. 5 Câu 23: Cho Glyxin NaOH X HCl Y ; Glyxin HCl Z NaOH T. Y và T lần lượt là: A. Đều là ClH3NCH2COONaB. ClH 3NCH2COOH và ClH3NCH2COONa Hướng dẫn giải mX =mY= mtăng + mZ => mtăng = mX - mz; mZ = 2.10,08.0,28/22,4 = 0,252g mtăng = 0,02.26 + 0,03.2 – 0,252 = 0,328g Câu 31: Khối lượng của một đoạn nilon – 6,6 là 27346 đvC và một đoạn mạch tơ capron là 17176 đvC. Số lượng mắt xích trong đoạn mạch của 2 polime nêu trên lần lượt là? A. 113 và 152B. 121 và 114C. 121 và 152D. 113 và 114 Câu 32: Thí nghiệm 1: Cho a mol Al2(SO4)3 tác dụng với 500ml dung dịch NaOH 1,2M được m gam kết tủa. Thí nghiệm 2: Cũng a mol Al2(SO4)3 tác dụng với 750ml dung dịch NaOH 1,2M thu được m gam kết tủa. Tính a và m? Hướng dẫn giải Vì cùng một lượng ion Al 3+ phản ứng với lượng OH - khác nhau nhưng ở cả 2 thí nghiệm đều thu được lượng kết tủa bằng nhau nên: n - TN1: Al3+ dư, OH- hết. ↓ n n OH = 0,2 mol→m = 15,6 gam. Al(OH )3 3 - TN2: Kết tủa sinh ra bị hòa tan 1 phần. Áp dụng công thức: nOH- 0,6 0,9 3+ - 3+ 3+ n↓còn lại = 4nAl - nOH → 0,2 = 4nAl - 0,9 → nAl = 0,275 mol. Vậy a = 0,275/2 = 0,1375 mol. Mức độ vận dụng cao gồm 08 câu ( từ câu 33 đến câu 40) Câu 33: Đốt cháy hoàn toàn 10,58 gam hỗn hợp X chứa ba este đều đơn chức, mạch hở bằng lượng oxi vừa đủ, thu được 8,96 lít khí CO2 (đktc). Mặt khác, hidro hóa hoàn toàn 10,58 gam X cần dùng 0,07 mol o H2 (xúc tác, t ) thu được hỗn hợp Y. Đun nóng toàn bộ Y với 250 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được một ancol Z duy nhất và m gam rắn khan. Gía trị của m là : A. 15,45 gam B. 15,6 gam C. 15,46 gam D. 13,36 gam Hướng dẫn giải Hidro hóa hoàn toàn hỗn hợp X thì : mY mX 2nH2 10,72(g) - Giả sử đốt cháy hoàn toàn hỗn hợp Y (CTTQ của Y là C nH2nO2) thì : mY 12nCO2 2nH2O + nCO nH O 0,4 mol nY n COO 0,16 mol 2 2 32 nCO2 - Ta có : C Y 2,5. Vậy trong Y có chứa este HCOOCH3 nY - Khi cho lượng Y trên tác dụng với 0,25 mol NaOH thì ancol Z thu được là CH 3OH BTKL với nCH3OH nY 0,16 mol mr¾n khan mY 40nNaOH 32nCH3OH 15,6(g) 0,06x'+0,04y'=0,26 3x'+2y'=13 x'=3; y'=2 (x'=1; y'=5 Loại) Kết luận: X có dạng Gly-Gly-Gly-Ala M(X)=260; Y: Gly-Gly-Ala-Ala-Ala M(Y)=345 0,04*345 %Y : 0,46938 47% 0,04*345 0,06* 260 Câu 37: Nung 23,2 gam hỗn hợp X ( FeCO 3 và FexOy ) tới phản ứng hoàn toàn thu được khí A và 22,4 gam Fe2O3 duy nhất. Cho khí A hấp thụ hoàn toàn vào dung dịch Ba(OH) 2 dư thu được 7,88 gam kết tủa. Mặt khác , để hòa tan hết 23,2 gam X cần vừa đủ V ml dung dịch HCl 2M. CT FexOy và giá trị của V là : A. 240 lít.B. 360 lít. C. 170 lít. D. 120 lít Hướng dẫn giải nFeCO3 = nCO2 = nBaCO3 = 7,88/197 = 0,04 mol. BTNT Fe : ∑nFe = 2nFe2O3 = 0,28 mol => nFe(oxit) = 0,28 – 0,04 = 0,24 mol => moxit = mX – mFeCO3 = 23,2 – 0,04.16 = 18,56 gam => nO (oxit ) = ( 18,56 – 0,24.56 ) / 16 = 0,32 mol => Fe3O4 . BTĐT : nHCl = nH+ = 2nCO3(2-) + 2 nO (oxit ) = 2.0,04 + 2.0,32 = 0,72 mol => V = 0,72/2 = 0,36 lit = 360 ml Câu 38: Một hợp chất hữu cơ X có công thức phân tử C 10H8O4 trong phân tử chỉ chứa 1 loại nhóm chức. Cho 1 mol X phản ứng vừa đủ với 3 mol NaOH tạo thành dung dịch Y gồm 2 muối (trong đó có 1 muối có M<100), 1 anđehit no (thuộc dãy đồng đẳng của metanal) và nước. Cho dung dịch Y phản ứng với lượng dư AgNO3/NH3 thì khối lượng kết tủa thu được gần nhất là: A. 161.19 gamB. 431,19 gam C. 162 gam D. 108,19 gam Hướng dẫn giải X: HOOC6H4COOCH=CH2 + 3NaOH => HCOONa + C6H4COONa + CH3CHO Y + AgNO3 + NH3 HCOONa => 2Ag ; CH3CHO => 2Ag => m Ag = 432g => Chọn B 2+ + – – – Câu 39: Dung dịch X chứa các ion: Ca , Na , HCO3 và Cl , trong đó sốmol của ion Cl là 0,1. Cho 1/2 dung dịch X phản ứng với dung dịch NaOH (dư), thu được 2 gam kết tủa. Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2(dư), thu được 3 gam kết tủa. Mặt khác, nếu đun sôi đến cạn dung dịch X thì thu được m gam chất rắn khan. Giá trịcủa m là A. 7,47 gam B. 9,21 gam C. 8,79 gam D. 9,26 gam Hướng dẫn giải 1 2+ Từ giả thiết: dd X nếu thêm Ca(OH) 2 thì vẫn thu được thêm kết tủa nên Ca ban đầu thiếu và bằng số 2 2 mol kết tủa: n 2.n 2. 0,04(mol) Ca2 100 1 3 dd X thêm Ca(OH)2 thu kết tủa : n - 2.n(2) 2. 0,06(mol) 2 HCO3 100
File đính kèm:
 de_minh_hoa_thi_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2018_2019.doc
de_minh_hoa_thi_thpt_quoc_gia_mon_hoa_hoc_nam_hoc_2018_2019.doc

