Đề kiểm tra học kỳ II môn Hóa học 8 - Năm học 2015-2016 (Có đáp án)
Bạn đang xem tài liệu "Đề kiểm tra học kỳ II môn Hóa học 8 - Năm học 2015-2016 (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề kiểm tra học kỳ II môn Hóa học 8 - Năm học 2015-2016 (Có đáp án)
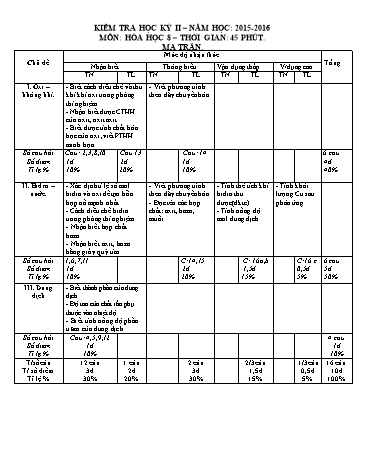
KIỂM TRA HỌC KỲ II – NĂM HỌC: 2015-2016 MÔN: HÓA HỌC 8 – THỜI GIAN: 45 PHÚT. MA TRẬN. Mức độ nhận thức Chủ đề Tổng Nhận biết Thông hiểu Vận dụng thấp V/dụng cao TN TL TN TL TN TL TN TL I. Oxi – - Biết cách điều chế và thu - Viết phương trình không khí. khí khí oxi trong phòng theo dãy chuyển hóa. thí nghiệm. - Nhận biết được CTHH của oxit, oxit axit. - Biết được tính chất hóa học của oxi ,viết PTHH minh họa Số câu hỏi Câu: 2,3,8,10 Câu 13 Câu: 14 6 câu Số điểm 1đ 2đ 1đ 4đ Tỉ lệ % 10% 20% 10% 40% II. Hiđro – - Xác định tỉ lệ số mol - Viết phương trình - Tính thể tích khí - Tính khối nước. hiđro và oxi để tạo hỗn theo dãy chuyển hóa. hiđro thu lượng Cu sau hợp nổ mạnh nhất. - Đọc tên các hợp được(đktc) phản ứng - Cách điều chế hiđro chất: axit, bazơ, - Tính nồng độ trong phòng thí nghiệm. muối. mol dung dịch - Nhận biết hợp chất bazơ. - Nhận biết axit, bazơ bằng giấy quỳ tím. Số câu hỏi 1,6,7,11 C:14,15 C: 16a,b C:16 c 6 câu Số điểm 1đ 2đ 1,5đ 0,5đ 5đ Tỉ lệ % 10% 20% 15% 5% 50% III. Dung - Biết thành phần của dung dịch dịch. - Độ tan của chất rắn phụ thuộc vào nhiệt độ. - Biết tính nồng độ phần trăm của dung dịch. Số câu hỏi Câu: 4,5,9,12 4 câu Số điểm 1đ 1đ Tỉ lệ % 10% 10% T/số câu 12 câu 1 câu 2 câu 2/3câu 1/3câu 16 câu T/ số điểm 3đ 2đ 3đ 1,5đ 0,5đ 10đ Tỉ lệ % 30% 20% 30% 15% 5% 100% KIỂM TRA HỌC KỲ II – NĂM HỌC: 2015-2016 MÔN: HÓA HỌC 8. ĐÁP ÁN – BIỂU ĐIỂM. ĐỀ 1. I. TRẮC NGHIỆM: (3 điểm). Mỗi câu đúng 0.25 điểm. Câu 1 2 3 4 5 6 7 8 9 10 11 12 Đáp án D B A C C A D B D B A C II. TỰ LUẬN: (7 điểm) Câu Đáp án Điểm Câu 1 * Tính chất hóa học của oxi: (2 điểm) - Tác dụng với phi kim. 0,25đ to PTHH: S + O2 SO2 0,5đ - Tác dụng với kim loại. 0,25đ to 0,5đ PTHH: 3Fe + 2O2 Fe3O4 - Tác dụng với hợp chất. 0,25đ to 0,25đ PTHH: CH4 + 2O2 CO2 + 2H2O t0 .Câu 2 a. 2KClO3 2KCl + 3O2. 0,5đ (1,5 điểm) b. O2 + Na Na2O. 0,.5đ 0,5đ c. Na2O + H2O NaOH . Câu 3 - Axit: HCl: Axit Clohiđric. 0,25đ (1,5 điểm) H2SO4: Axit Sunfuric 0,25đ - Bazơ: KOH: Kali hiđroxit. 0,25đ Fe(OH)3: Sắt (III) hiđroxit. 0,25đ - Muối: CaCl2: Canxi Clorua. 0,25đ ZnSO4: Kẽm Sunfat. 0,25đ Câu 4 Số mol của Magie: nMg = m : M = 4,8 : 24 = 0,2 (mol) 0,25đ (2 điểm) PTHH: Mg + 2HCl MgCl2 + H2 0,25đ Theo PTHH: n H2 = nMg =0,2 (mol) 0,25đ nHCl = 2nMg =0,4 (mol) 0,25đ a. VH2 = n . 22,4 = 0,2 . 22,4 = 4,48 (l) 0,25đ b CM(HCl) = 0,4 / 0,2 = 2M 0,25đ c. Số mol của đồng (II) oxit là: nCuO = 20 : 80 = 0,25(mol) t0 PTHH: CuO + H2 Cu + H2O 0,25đ 1 1 1 1 (mol) Xét tỉ lệ: 0,25:1 > 0,2:1 => CuO dư, tính theo số mol H2 0,25đ Theo PTHH nCu = nH2 = 0,2 (mol) mCu = 0,2 .64 =12,8 (g)
File đính kèm:
 de_kiem_tra_hoc_ky_ii_mon_hoa_hoc_8_nam_hoc_2015_2016_co_dap.doc
de_kiem_tra_hoc_ky_ii_mon_hoa_hoc_8_nam_hoc_2015_2016_co_dap.doc

